Манай улс хүн амаа дархлаажуулахдаа дөрвөн төрлийн вакциныг ашиглаж буй. Үүнд:
- Их Британийн “АстраЗенека”компани болон Оксфордын их сургуулийн эрдэмтдийн хамтран бүтээсэн “AZD1222” “Covishield” вакцин
- Америкийн эмийн үйлдвэрийн томоохон компани “Pfizer”болон Германы “BioNTech” компаниуд хамтран “BNT162b2”
- ОХУ-д үйлдвэрлэсэн “Спутник V”
- БНХАУ-д үйлдвэрлэсэн “Синифарм” үйлдвэрийн “Веросел”. Эдгээрээс ДЭМБ-аас “АстраЗенека” болон “Pfizer” үйлдвэрийн вакцинд зөвшөөрөл олгосон бол урд болон хойд хөршийн вакцинд хараахан зөвшөөрөл олгоогүй, туршилт судалгааны үр дүнг нь үнэлэх ажлууд явагдаж байна.
|
|
Үйлдвэрийн технологи |
Хийх тун |
Үр дүн |
Хадгалах нөхцөл |
Нэг тунгийн үнэ/Импортлогчоос хамаарч үнэ нь янз бүр байж болно/ |
|
"АстраЗенека" |
Векторийн вируст суурилсан |
4-12 долоо хоногийн зайтай-2 тун |
70 хувь |
2-8 хэм |
2.16-5.25 ам.доллар |
|
“Спутник V” |
Аденовируст суурилсан |
21 хоногийн зайтай-2 тун |
91.6 хувь |
2-8 хэм |
10 ам.доллар |
|
"Файзер" |
РНХ уурагт суурилсан |
21 хоногийн зайтай-2 тун |
95 хувь |
-70 хэм
|
14-20 ам.доллар |
|
"Синофарм" |
Идэвхигүйжүүлсэн вирус |
4 долоо хоногийн зайтай- 2 тун |
79-86 хувь |
+4+8 хэм |
5-32 ам.доллар |
Хэд хоногийн өмнө БНХАУ-д үйлдвэрлэсэн “Синофарм” вакциныг элэгний В,С вирустэй хүмүүст хийлгэж болохгүй гэх мэдээллийг ЭМЯ-аас өгсөн боловч маргааш нь дахин залруулга хийсэн. Тодруулбал, элэгний ээнэгшил алдагдаагүй, хүнд хэлбэрийн биш бол тус вакциныг хийлгэх боломжтой хэмээн тайлбарласан юм. Үүнээс улбаатай иргэдийн дунд багагүй эргэлзээ үүсээд байна. Тиймээс манай улс дархлаажуулалтдаа хэрэглэж буй дээрх дөрвөн вакцины эсрэг заалт болон ямар хүнд хийж болох, болохгүй талаар ДЭМБ, Европын эмийн агентлаг зэрэг олон улсын байгууллагуудын гаргасан судалгааг хүргэж байна.
-“АСТРАЗЕНЕКА” КОМПАНИ, ОКСФОРДЫН ИХ СУРГУУЛИЙН ХАМТРАН БҮТЭЭСЭН “AZD1222” БУЮУ COVISHIELD” ВАКЦИН-
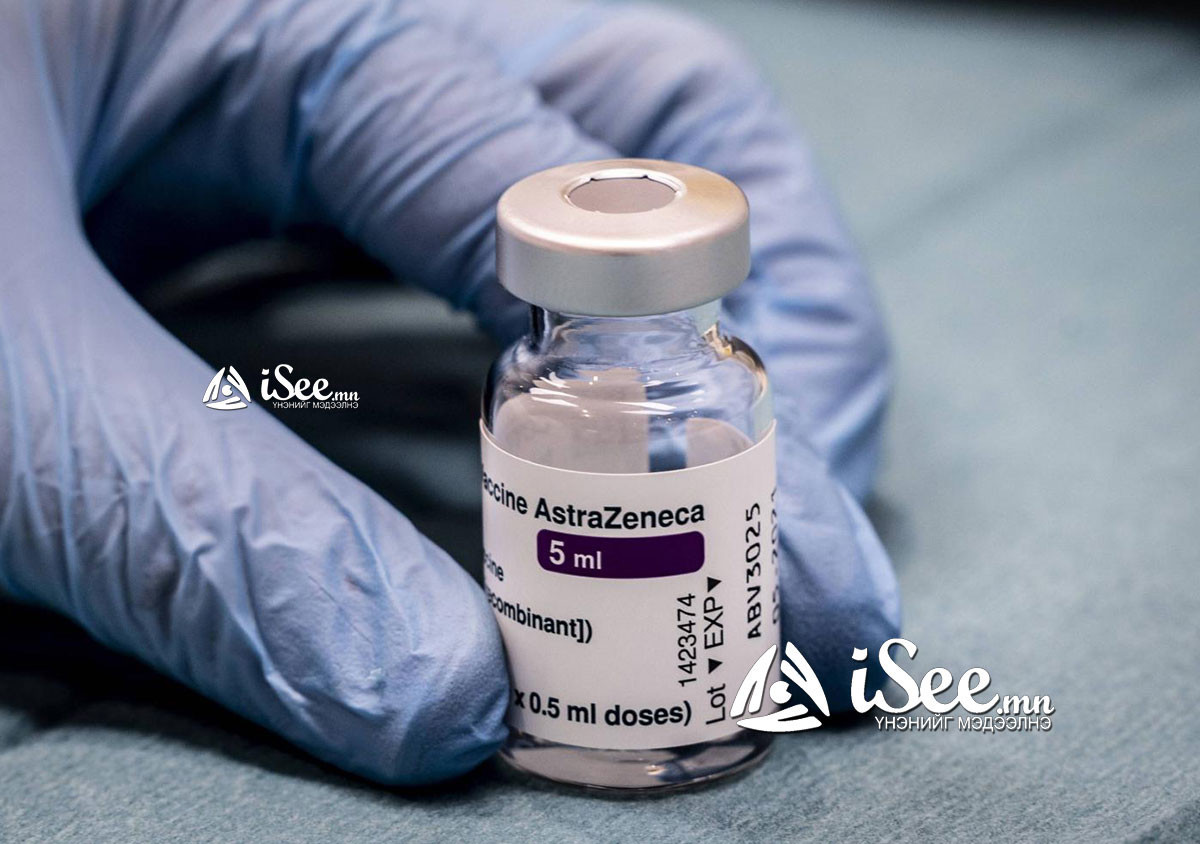
Ерөнхийдөө бүх вакцины заалтад найрлагад орсон аль нэг бодис, бүрэлдэхүүн хэсгээс харшилтай бол хийхийг хориглосон байдаг. Үүний адилаар ДЭМБ-аас гаргасан “Оксфордын Их Сургууль, AstraZeneca-ийн боловсруулсан COVID-19-ийн эсрэг AZD1222 (ChAdOx1-S [рекомбинант]) вакциныг ашиглах түр зөвлөмж”-д өгүүлснээр Вакцины аль нэг бүрэлдэхүүн хэсэгт анафилакси/харшил/ үзүүлж байсан түүх нь вакцинжуулалтын эсрэг заалт юм. Энэ вакцины эхний тунг тариулсны дараа анафилаксийн урвал үзүүлсэн хүмүүс тухайн вакцины хоёр дахь тунг хийлгэж болохгүй” хэмээн бичжээ. Үүнээс гадна халууралттай цочмог өвчтэй хүн (биеийн температур 38.5 С-ээс дээш) вакцин хийлгэх хугацаагаа халуун бууртал хойшлуулах хэрэгтэй. Гэсэн хэдий ч хөнгөн ханиад, бага зэрэг халуурах шинж тэмдгийн улмаас вакцинжуулалтыг хойшлуулах ёсгүй.
Эмнэлзүйн туршилтад хамрагдсан хавсарсан өвчинд таргалалт, зүрх судасны өвчин, амьсгалын замын өвчин, чихрийн шижин зэрэг оржээ. Хүнд хэлбэрийн COVID-19-ийн эрсдлийг нэмэгдүүлдэг нь тогтоогдсон хавсарсан өвчтэй хүмүүст вакцин хийлгэхийг зөвлөж байна.
Эмнэлзүйн туршилтуудаас авах мэдээлэл хязгаарлагдмал эсвэл огт байхгүй хүн ам 18-аас доош насны хүүхэд, өсвөр насныхан. Одоогийн байдлаар 18 нас хүрээгүй хүүхэд, өсвөр насныханд вакцины үзүүлэх үр нөлөө, аюулгүй байдлын талаарх мэдээлэл алга байна. Ийм мэдээлэл гартал 18-аас доош насны хүмүүст вакцин хийлгэхийг зөвлөхгүй.
Жирэмсэн эмэгтэйчүүдэд төрөх насны жирэмсэн бус эмэгтэйчүүдийг бодвол COVID19-ийн хүнд хэлбэрийн эрсдэл өндөр байдаг ба COVID-19 нь дутуу төрөх эрсдэлийг нэмэгдүүлдэг ажээ. Вакцины үр нөлөө эсвэл жирэмсэн үеийн вакцинтай холбоотой эрсдэлийг үнэлэхэд жирэмсэн эмэгтэйчүүдийн AZD1222 вакцинжуулалтын мэдээлэл хангалтгүй байна.
Хөхүүл эмэгтэйчүүд. Хөхөөр хооллох нь хөхүүл эмэгтэйчүүд болон тэдний хөхүүл хүүхдүүдэд эрүүл мэндэд ихээхэн ач тустай байдаг. Хөхүүл эмэгтэйчүүдэд үзүүлэх вакцины үр нөлөө нь бусад насанд хүрэгчдийнхтэй адил байх төлөвтэй байна. “AZD1222” нь эхийн сүүгээр ялгардаг эсэх нь тодорхойгүй байна. AZD1222 вакцин нь репликацид ордоггүй вакцин тул хөхүүл хүүхдэд эрсдэл учруулахгүй байх магадлалтай. Эдгээр үзэл санаан дээр үндэслэн хэрэв хөхүүл эмэгтэй нь вакцин хийлгэхийг зөвлөж буй бүлгийн нэг хэсэг бол, жишээ нь эрүүл мэндийн ажилтан бол түүнд бусадтай адил 7/15 вакцинжуулалтыг санал болгох хэрэгтэй. ДЭМБ вакцин хийлгэсний дараа хөхөөр хооллохоо зогсоох зөвлөмж гаргаагүй байна.
Аутоиммун өвчтэй хүмүүс. Аутоиммун өвчтэй хүмүүст AZD1222-ийн аюулгүй байдал, үр дүнтэй байдлын талаар одоогоор мэдээлэл алга байна. Вакцин хийлгэхийг зөвлөж буй бүлгийн нэг хэсэг болох аутоиммун өвчтэй хүмүүсийг вакцинжуулж болох юм.
Цочмог COVID-19-р одоо өвчилсөн байгаа хүмүүс PCR-аар батлагдсан цочмог COVID-19-тэй хүмүүс, түүний дотор тунгийн хооронд халдвар авсан нь PCR-р батлагдсан хүмүүст вакцин хийхийг цочмог өвчнийг нь эдгэртэл, тусгаарлалтыг зогсоох шалгуурыг хангаж дуустал хойшлуулах шаардлагатай. SARS-CoV-2-ийн халдвар авсан нь PCR-аар батлагдсан хүмүүс вакцинжуулалтыг 6 сараар хойшлуулж болно. Байгалийн халдварын дараа тогтсон дархлааны үргэлжлэх хугацааны талаарх нэмэлт мэдээлэл гарахад вакцин хойшлуулалтын үргэлжлэх хугацааг шинэчилж болох юм.
Өмнө нь COVID-19-ийн эсрэгбиеийн идэвхгүй эмчилгээ хийлгэсэн хүмүүс COVID-19-ийн эмчилгээний нэг хэсэг болох моноклональ эсрэгбие эсвэл эдгэрсэн хүний сийвэн тариулсан хүмүүст вакцин хийхэд аюулгүй байдал, үр дүнгийн талаархи мэдээлэл одоогоор алга байна. Тиймээс вакцинаас үүдэлтэй дархлааны хариу урвал нь эсрэгбиеийн эмчилгээтэй харшилдахгүйн тулд урьдчилан сэргийлэх зорилгоор вакцинжуулалтыг дор хаяж 90 хоног хойшлуулах хэрэгтэй.
ДЭМБ-аас гаргасан тус вакцины зөвлөмжид ийн бичжээ. Харин “АстраЗенека” компаниас гаргасан тайлан, судалгаанд элэгний В,С вирустэй хүмүүст хориглох заалт тэмдэглэгдээгүй байна.
-ДЭМБ-ААС БАТАЛГААЖУУЛСАН АНХНЫ ВАКЦИН БОЛОХ “PFIZER”-ЭЛЭГНИЙ В,С ВИРУС, ХДХВ-ТЭЙ ХҮМҮҮС ХИЙЛГЭЖ БОЛНО-
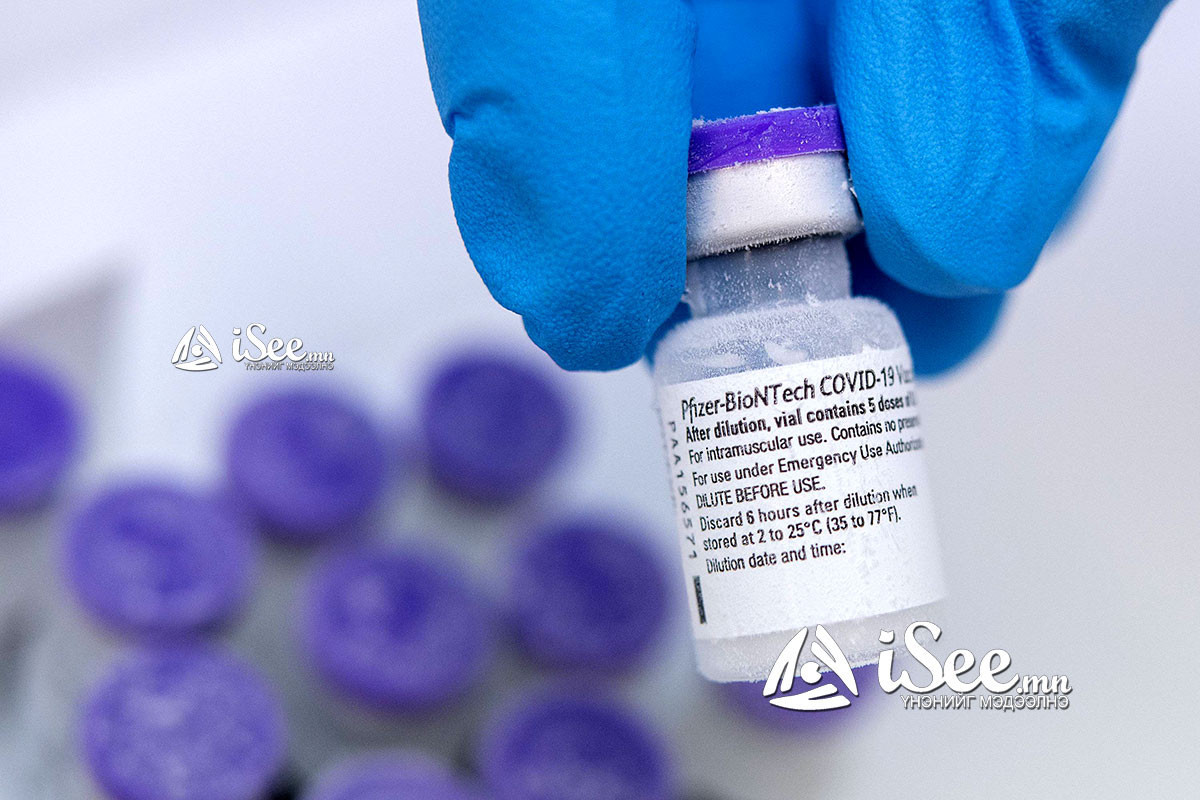
"Файзер" бол уламжлалт аргын вакцин биш, харин уургийн мэдээллийг агуулсан РНХ-г /рибонуклейн хүчил/ шууд вакцин болгон ашиглахад чиглэсэн хамгийн сүүлийн үеийн технологиор гарган авсан вакцин юм.Манай улсын хувьд “Pfizer”/“BNT162b2”/ вакциныг энэ сарын 26-аас эхлэн дархлаажуулалтдаа хэрэглэж эхлээд байна. Ингэхдээ эрхтэн шилжүүлэн мэс засал хийлгэсэн, донор хүмүүст хийж буй. Тэгвэл “Pfizer” вакцины эсрэг заалтын талаар нарийвчилсан судалгааг танилцуулъя.
Вакцины эсрэг заалт. Эсрэг заалт вакцины аль ч бүрэлдэхүүн хэсэгт харшлын урвал (жишээлбэл, анафилакс) үзүүлж байсан бол вакцинжуулалтын эсрэг заалт болно. Ялангуяа “BNT162b2”-ийн бүрэлдэхүүнд ордог полиэтилен гликол (PEG) эсвэл түүнтэй холбоотой молекулуудад харшилтай нь урьд өмнө мэдэгдэж байсан хүмүүст тарьж болохгүй. Учир нь PEG нь вакцины бүрэлдэхүүн хэсэг юм.
BNT162b2 вакцин хэрэглэсний дараа анафилаксийн урвал өгсөн гэж эмнэлзүйн туршилтаас гадуур бүртгэгдсэн байна. Бусад вакцин эсвэл тарилгын эмчилгээнд (булчинд, судсаар эсвэл арьсан доорх вакцин, эмчилгээ гэх мэт) шууд харшлын 5/15 урвал үзүүлж байсан түүхтэй бол анхаарах хэрэгтэй гэж үздэг боловч энэ нь вакцинжуулалтын эсрэг заалт биш юм. Ийм хүмүүсийг вакцин хийлгэсний дараа анафилаксийг даруй эмчилж болохуйц эрүүл мэндийн байгууллагын орчинд 30 минутын турш ажиглах ёстой. Ерөнхийдөө эхний тунг тарихад шууд харшлын урвал үзүүлсэн хүмүүст нэмэлт тунг хийх ёсгүй.
Вакцин хийснээс хэдэн цагийн дотор тохиолдсон вакцин эсвэл эмэнд шууд үзүүлэх харшлын урвалыг хэт мэдрэгшилтэй холбоотой шинж тэмдэг, тухайлбал анафилакси, чонон хөрвөс, ангиоэдема, амьсгалын замын хямрал (жишээлбэл, хэржигнэх, хяхтнах) гэж тодорхойлсон болно. Гэсэн хэдий ч хэрэв энэ нь хүнд хэлбэрийн COVID-19-ийн эрсдэл өндөртэй хүмүүст боломжтой дархлаажуулалтын мэргэшсэн үйлчилгээний цорын ганц сонголт бол эрсдэл үр ашгийн үнэлгээг харгалзан үзэж, BNT162b2-ийг эмнэлгийн нарийн хяналтан дор хийхийг зөвшөөрнө.
Халууралттай цочмог өвчтэй хүн (биеийн температур 38.5oС-ээс дээш) вакцин хийлгэх хугацаагаа халуун бууртлаа хойшлуулах хэрэгтэй.
Хавсарсан өвчтэй хүмүүс. ДЭМБ-аас COVID-19-ийн хүнд хэлбэрийн өвчлөл, нас баралтын эрсдэлийг нэмэгдүүлдэг тодорхой хавсарсан өвчнүүдийг тогтоосон байна. Эмнэлзүйн 2/3-р шатны туршилтуудаар вакцин нь янз бүрийн суурь өвчтэй хүмүүст, түүний дотор хүнд хэлбэрийн COVID-19-ийн эрсдэлтэй хүмүүст аюулгүй байдал, үр ашгийн хувьд ижил нөлөөтэй болохыг нотолжээ. Эмнэлзүйн туршилтын 2/3 үе шатанд судлагдсан хавсарсан эмгэгүүд нь даралт ихсэлт, чихрийн шижин, багтраа, уушиг, элэг, бөөрний өвчин, хүний дархлал хомстолын вирус (ХДХВ), гепатит С вирус (HCV) ба гепатит В вирус (HBV) -ын архаг (тогтвортой, хяналттай) халдвар юм. Хүнд хэлбэрийн COVID-19-ийн эрсдэлийг нэмэгдүүлдэг нь тогтоогдсон хавсарсан өвчтэй хүмүүст вакцин хийлгэхийг зөвлөмж болгож байна.
ХДХВ-ийн халдвартай хүмүүс. ХДХВ-ийн халдвартай хүмүүс COVID-19-ийн хүнд хэлбэрээр өвчлөх эрсдэл өндөр байж болно. ХДХВ-ийг сайн хянаж буй 2/3-р үе шатны эмнэлзүйн туршилтад оролцогчдын дунд аюулгүй байдлын дохиоллын хувьд ялгаа бүртгэгдээгүй байна. Вирусийн эсрэг эмчилгээнд сайн хяналттай байгаа, вакцинд хамрагдахыг зөвлөж буй бүлгийн нэг хэсэг болох ХДХВ-ийн халдвартай хүмүүсийг вакцинжуулах боломжтой.
Нүүрний захын мэдрэлийн саажилтын түүхтэй хүмүүс. Pfizer-BioNTech эмнэлзүйн туршилтад оролцогчдод вакцин хийлгэсний дараа нүүрний захын мэдрэлийн саажилтын тохиолдол бүртгэгдсэн байна. Гэсэн хэдий ч эдгээр тохиолдлууд нь вакцинжуулалттай холбоотой эсэхийг нотлох баримт одоогоор алга байна. Зөвшөөрлийн дараах аюулгүй байдлын тандалт нь болзошгүй аливаа шалтгаан хамаарлын холбоог үнэлэхэд чухал ач холбогдолтой юм. Ийм нотлох баримт байхгүй тохиолдолд нүүрний захын мэдрэлийн саажилтын түүхтэй хүмүүс вакцинжуулалтын эсрэг заалт байхгүй тохиолдолд BNT162b2-ийг хийлгэж болно.
Өмнө нь COVID-19-ийн эсрэгбиеийн идэвхгүй эмчилгээ хийлгэсэн хүмүүс. COVID-19-ийн эмчилгээний нэг хэсэг болох моноклональ эсрэг бие эсвэл эдгэрсэн хүний сийвэн тариулсан хүмүүст вакцин хийхэд аюулгүй байдал, үр дүнгийн талаарх мэдээлэл одоогоор алга байна. Тиймээс вакцинаас үүдэлтэй дархлааны хариу урвал нь эсрэгбиеийн эмчилгээтэй харшилдахгүйн тулд урьдчилан сэргийлэх зорилгоор вакцинжуулалтыг дор хаяж 90 хоног хойшлуулах хэрэгтэй.
Аутоиммун өвчтэй хүмүүс. Вакцинжуулалтын эсрэг заалтгүй аутоиммун өвчтэй хүмүүс хийлгэж болно.
-ОХУ-ЫН СПУТНИК V ВАКЦИНЫ ЭСРЭГ ЗААЛТ-
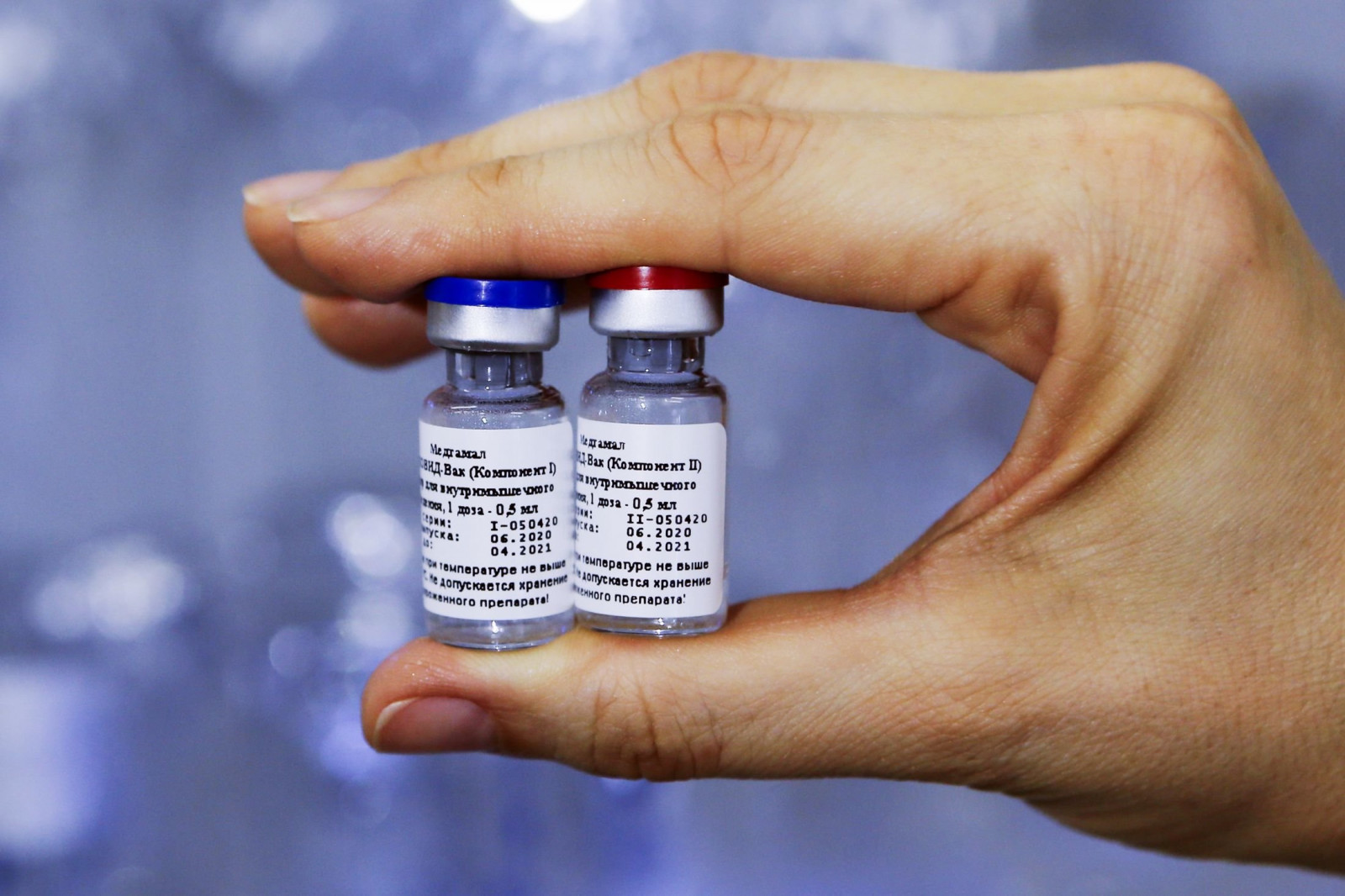
ДЭМБ-аас ОХУ-д үйлдвэрлэсэн “Спутник V” вакцинд зөвшөөрөл олгоогүй тул албан ёсны тайлан, мэдээлэл хомс байна. Гэсэн хэдий ч судалгааны ажил үргэлжилж байгаа талаар ОХУ-ын хэвлэлүүд бичжээ.
Москва дахь Н.Ф.Гамалеягийн нэрэмжит Халдвар судлал, бичил биологийн эрдэм шинжилгээний төвийн эрдэмтдийн гарган авсан “Спутник – V” /Гам-КОВИД-Вак/ вакцин бол 90-ээс дээш хувийн үр дүн /91,6%/ үзүүлсэн гурван вакцины нэг юм. Эмнэл зүйн туршилтын 3 дугаар үе шат нь дуусаагүй байхад өнгөрсөн оны 8 дугаар сард ОХУ-ын зохицуулагч байгууллага уг вакциныг бүртгэн авч, улмаар 12 дугаар сараас хэрэглэж эхэлсэн нь эргэлзээ дагуулж, барууны хэвлэлүүдийн хүчтэй шүүмжлэлд өртөж байсан билээ.
Оросын вакцин нь “SARS-CoV-2” вирусийн өргөсний уургийн геномийг агуулсан аденовирусийн вектор дээр суурилагдсан бөгөөд энэ нь олон арван жилийн туршид сайтар судлагдсан платформ учраас аюулгүй байх учиртай. Энэхүү платформыг Эбола, MERS өвчний эсрэг вакцин гарган авахад ашиглаж байжээ.
Вакцины эсрэг заалт. Өнгөрсөн хоёрдугаар сард Гамалеягийн хүрээлэнгийн захирал А.Гинцбург дараах гурван хүнд “Спутник V” вакциныг хориглож байв. Үүнд:
- Жирэмсэн болон хөхүүл хүүхэдтэй эхчүүд,
- Ойрын 3 сарын дотор жирэмслэхээр төлөвлөж буй залуу эхчүүд,
- Хавдар, сүрьеэ, сифилис гэх мэт тодорхой өвчнөөр өвчилж буй тохиолдолд вакцинд хамрагдахгүй байх нь зүйтэй гэжээ.
Үүнээс гадна вакцин хийлгэхээс өмнө болон дараа 45 хоногийн хугацаанд согтууруулах ундааны зүйл хэрэглэхийг хориглоно гэж хэлсэн нь нэлээдгүй маргаан дагуулсан юм. Зарим хүмүүс үүнийг “биелүүлэх боломжгүй хэт өндөр шаардлага” гэж үзэж байгаа бол дархлаа судлаач эмч В.Болибок-ийн ярьснаар “вакцины тун бүрийг хийлгэхээс 3 хоногийн өмнө, хийлгэсний дараа 3 хоногийн хугацаанд архи уухгүй байх нь зүйтэй. Энэ бол арай илүү бодитой шаардлага” гэжээ.
Дэлхийн хэмжээнд хийгдсээр байгаа судалгааны үр дүнд “Sputnik-V” вакцин хийлгэсэн нийт хүмүүсийн 10 орчим хувьд нь “SARS-CoV-2” вирусийн эсрэг дархлаа тогтохгүй байгаа бөгөөд энэ тоо бусад вакцины хувьд харилцан адилгүй байгаа юм. Тухайлбал, “Sputnik-V” вакцин үр дүн 91.6 хувь, “Pfizer/BioNTech” – 95 хувь, “Moderna” – 94.1 хувь, “AstraZeneca” – 72 хувь, “Sinopharm” – 80-90 хувийн үр дүнд хүрсэн. Чухам ямар хүнд “COVID-19”-ийн эсрэг вакцин тариулсны дараа дархлаа тогтохгүй байгаа нь тодорхойгүй байгаа бөгөөд үүнд тухайн хүний алкоголийн хэрэглээ нөлөөлж байгаа эсэхийг хараахан судалж үзээгүй байгаа юм.
Үүнээс гадна хүрээлэнгээс гаргасан зөвлөмжид коронавирусийн халдвар авч, өвчлөл үргэлжилж байгаа хүмүүс, маш ховор тохиолддог харшлын урвал үзүүлдэг нь тогтоогдсон хүмүүс, маш ховор тохиолддог харшлын урвал үзүүлдэг нь тогтоогдсон хүмүүс уг вакциныг хийлгэхгүй гэжээ.
“Лансет” сэтгүүл дээр “Спутник” вакцины талаар мэдээлэл гарсан ч дутуу дулимаг бөгөөд судалгааны аргачлал нь вакциныг үр дүнтэй гэж гаргахаар хүчилсэн байдалтай байсан хэмээн эрдэмтэд шүүмжилсэн.
-СИНОФАРМ ВАКЦИН-ЭЛЭГ, БӨӨР, АМЬСГАЛЫН ЗАМ, ЗҮРХ СУДАСНЫ ӨВЧИН БОЛОН ХОРТ ХАВДРААР ХҮНДЭЭР ӨВЧИЛСӨН ХҮНД ХИЙХГҮЙ-
Хятад улс дотооддоо албан ёсоор бүртгэсэн "BBIBP-CorV" /Vero cell/ вакцин 79 хувийн үр дүн үзүүлсэн бол Арабын Нэгдсэн Эмират улсад хийсэн туршилт судалгаагаар эл үзүүлэлт 86 хувьд хүрсэн байна. Өнгөрсөн оны 7 дугаар сард уг вакциныг Хятадын хүн амын эрсдэл өндөртэй бүлгүүдэд яаралтай горимоор тарих шийдвэр гарчээ. Халдварт саа, улаан бурхны гээд бүх вакциныг гаргаж авсан уламжлалт аргад тулгуурласан, сулруулсан вирусийг агуулсан уг вакцинд сөрөг нөлөө бараг байхгүй гэж эрдэмтэд үзэж байна. Sinopharm группын ерөнхийлөгчийн мэдэгдсэнээр, уг вакцинаар 1 сая хүнийг тарьсны дараа ямар нэгэн хүндрэл, гаж нөлөө илрээгүй ажээ.
Хятадын клиник туршилтын бүртгэлд орсон “Vero Cell” вакцины зургаан тусдаа судалгааны өгөгдөлд дурдсанаар аюулгүй байдлын үүднээс дараах бүлгийн иргэдийг туршилтад хамруулаагүй байна. Үүнд:
- Харшил, таталт, эпилепси, энцефалопати, психозын өвчний түүхтэй эсвэл гэр бүлээс удамшсан ижил өвчний түүхтэй
- Вакцины найрлагад орсон аль нэг бодис, бүрэлдэхүүн хэсгээс харшилтай. Эсвэл цочмог харшлын урвал, чонон хөрвөс, арьсны экзем, амьсгаа давхцах, ангионеврозын хаван, хэвлийгээр өвдөх гэх мэт вакцины хүчтэй гаж урвал илэрч байсан түүхтэй.
- Дархлал хомстол, хорт хавдрын эмчилгээ, дархлаа дарангуйлах эмчилгээ хийлгэж байгаа. Эсвэл ХДХВ-ийн шалтгаант гипо дархлаа бүхий өвчтөнүүд, төрөлхийн болон удамшсан дархлааны өвчтэй
- Вакцинд хамрагдахаас дор хаяж нэг сарын өмнө өвөрмөц бус иммуноглобулинын тарилга хийлгэсэн
- Элэг, бөөр, амьсгалын зам, зүрх судасны өвчин болон хорт хавдраар хүндээр өвчилсөн. Эмийн хяналтаас гадуур чихрийн шижин өвчний хүндрэлтэй. Янз бүрийн архаг болон цочмог суурь өвчтэй. Арьсны халдварт, идээт болон харшлын өвчтэй (Үүнд элэгний гепатит “B” болон “C” вирусийн халдвараар өвчилсөн хүнийг тусгайлан онцлоогүй болно)
- Цочмог болон халдварт өвчний улмаас биеийн температур 37 хэмээс дээш халуурсан
- Жирэмсэн болон хөхүүл эмэгтэйчүүд
ДЭМБ өдийг хүртэл уг вакциныг хэрэглэх зөвшөөрлийг олгоогүй байна. Саяхан ДЭМБ-ын Монгол Улс дахь Суурин төлөөлөгч Сергей Диордица мэдэгдэхдээ, уг вакциныг яаралтай горимоор хэрэглээнд нэвтрүүлэх зөвшөөрөл олгох тухай асуудлыг судалж байна гэсэн юм.
Эх сурвалж: WHO, TheLancet, CDC, Pfizer, Риа Новости
























